
日机装株式会社、日本勃林格殷格翰株式会社与⾦泽⼤学医药保健研究域药学系的⽟井 郁⺒教授等人的研究组,成功研发了具有正常培养条件下无法观察到的肾脏功能的创新药物研究用人肾细胞『3D-RPTEC』。新开发的技术有望在创药研究领域中代替过去主要通过动物实验测试药物的细胞实验,并且为提高新药开发的效率做出贡献。
本研究结果已在2023年6⽉29⽇科学志『 Drug Metabolism and Disposition 』 (https://dmd.aspetjournals.org/content/early/2023/06/29/dmd.122.001171)刊登。

创药研究用人肾细胞,是通过用特殊的培养方法培养市售的人肾由来细胞,再现了至今为止难以观察到的肾脏功能,实际已经确认其具备约20种主要药物转运体※ 的机能。
在创药研究中,药物的评价(药物动态和毒性)主要是通过动物实验进行的, 然而从物种差异和爱护动物的角度出发,通过细胞实验代替动物实验,在“试验管内(=in vitro)”重现并进行评估是需求所向。由于评估是基于人类来源的肾细胞而非动物,除了能消除物种差异的问题,细胞实验比动物实验可以更快地从研发初期阶段获得数据,从而缩减药物研发时间和成本。然而,一直以来都没有能满足创药研究需求的人肾细胞。
与活体肾脏相比,传统的人肾细胞(HK-2细胞和初代近端小管上皮细胞)在通常的培养条件下会丧失许多肾脏特有的机能(Jenkinson et al., Eur J Physiol, 2012) 。因此,在创药研究时,很多情况下会通过动物实验对肾脏进行评估。本次研究中,将在平面培养中无法显现的人近端小管上皮细胞(RPTEC)的OAT1(有机阴离子转运蛋白1)的遗传基因作为指标,研究了培养条件,尝试改善了RPTEC的肾脏机能。制造球状细胞(以下简称3D-RPTEC) ,并在⼀定条件下经三维培养后,OAT1遗传基因显现量随培养天数上升,与人肾⽪质的mRNA显现量有相同程度的改善(图1)。对本细胞实施微阵列的网罗性遗传基因表达解析和蛋白质组学的网罗性蛋白质表达解析的结果表明,除OAT1外,监管部门评估所需的SLC转运体,比起平面培养,通过三维培养得到了改善,甚至在培养32天后仍能保持显现(图2)。
此外,在对来自三个不同供体的RPTEC进行三维培养的mRNA显现分析中,约17000个基因中有87%的基因仅有50%的CV%变异,表明3D-RPTEC是一种供体差异小,易于使用的细胞。作为药物评估的例子,实施了以细胞内ATP量(生存率)为指标的in vitro毒性试验。结果表明,显示药物转运体引起肾毒性的Cisplatin和Adefovir,浓度依赖性地使细胞内ATP量减少。其减少分别被OCT(有机阳离子转运体)的抑制剂Cimetidine、OAT(有机阴离子转运体)的抑制剂Probenecid所抑制(图3)。因此表明,3D-RPTEC在医药品开发中的药物动态和毒性评估中,是一种简便且高效的in vitro实验系列。
概括而言,通过RPTEC制造球状细胞,在一定条件下三维培养的具备肾脏主要功能之一的药物转运体与人肾脏的显现量相同,并可长期维持28天以上(专利第6995112号)。另外,3D-RPTEC 还可用于观察药物转运体引起的肾毒性。而且,不仅是药物转运体,蛋白质组学检测到的约4800种蛋白质中有90%的显现量与人肾脏中的显现量水平相同,这表明3D-RPTEC在医药品开发中的药物动态和毒性评估中,是一种简便且高效的in vitro实验系列。另外,不仅是创药研究,这种人类肾脏细胞还有望用于各种与肾脏有关的研究中。

在3D-RPTEC中(左图)OAT1遗传基因的显现量随着培养天数的增加而增加,并在培养10天后达到最大值。
上述照片(右图)由日机装拍摄。
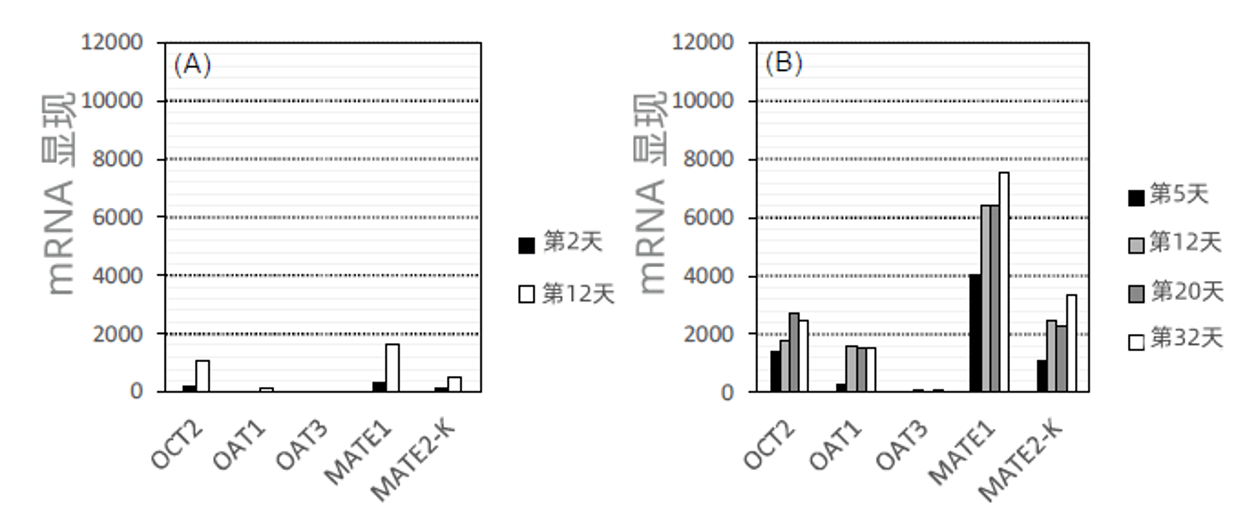
显示常规平面培养中RPTEC的遗传基因质显现量(A)和3D-RPTEC中的遗传基因显现量(B)。与常规平面培养相比,3D-RPTEC中药物转运体的显现量得到了改善,并且能够确定显现量从培养的第12天一直维持到第32天。
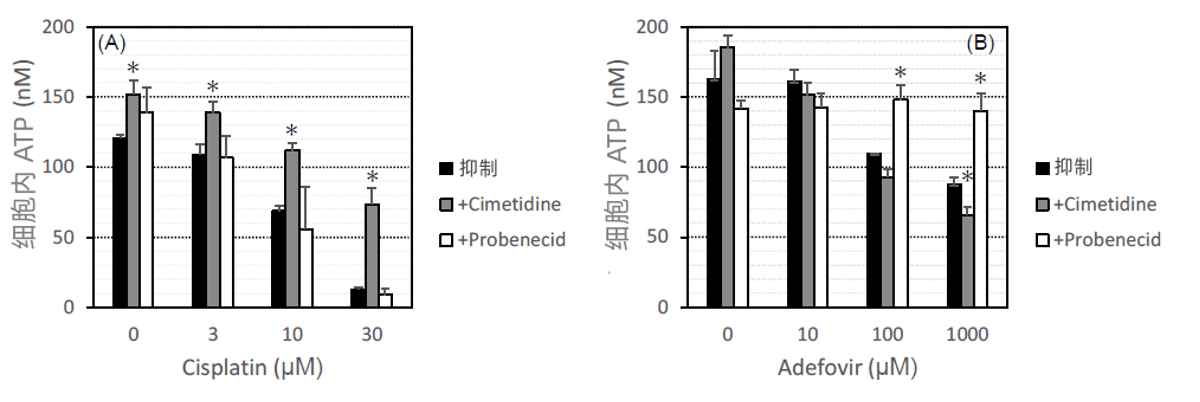
显示了在3D-RPTEC中暴露Cisplatin时细胞内ATP量(A)与暴露Adefovir时细胞内ATP量(B)。使用OCT及OAT的抑制剂,结果表明3D-RPTEC可检测出药物转运体引起的毒性。
根据本研究成果,⽇机装株式会社将创药研究用人肾细胞『3D-RPTEC®』产品化,于2023年7月开始正式销售。
今后,将3D-RPTEC作为肾脏评估的工具,在实验现场广泛应用,努力实现利用人肾细胞进行细胞实验的标准化。